Дано термохимическое уравнения: 2Н2O=2H2+O2-571,6кДж...Для проведения этой реакции затрачивается 285,5кДж теплоты . Сколько молей воды при этом разложится ????
Ответы на вопрос
Ответил smardoyan1998
0
Вот посмотри!!!!!!!!
Приложения:
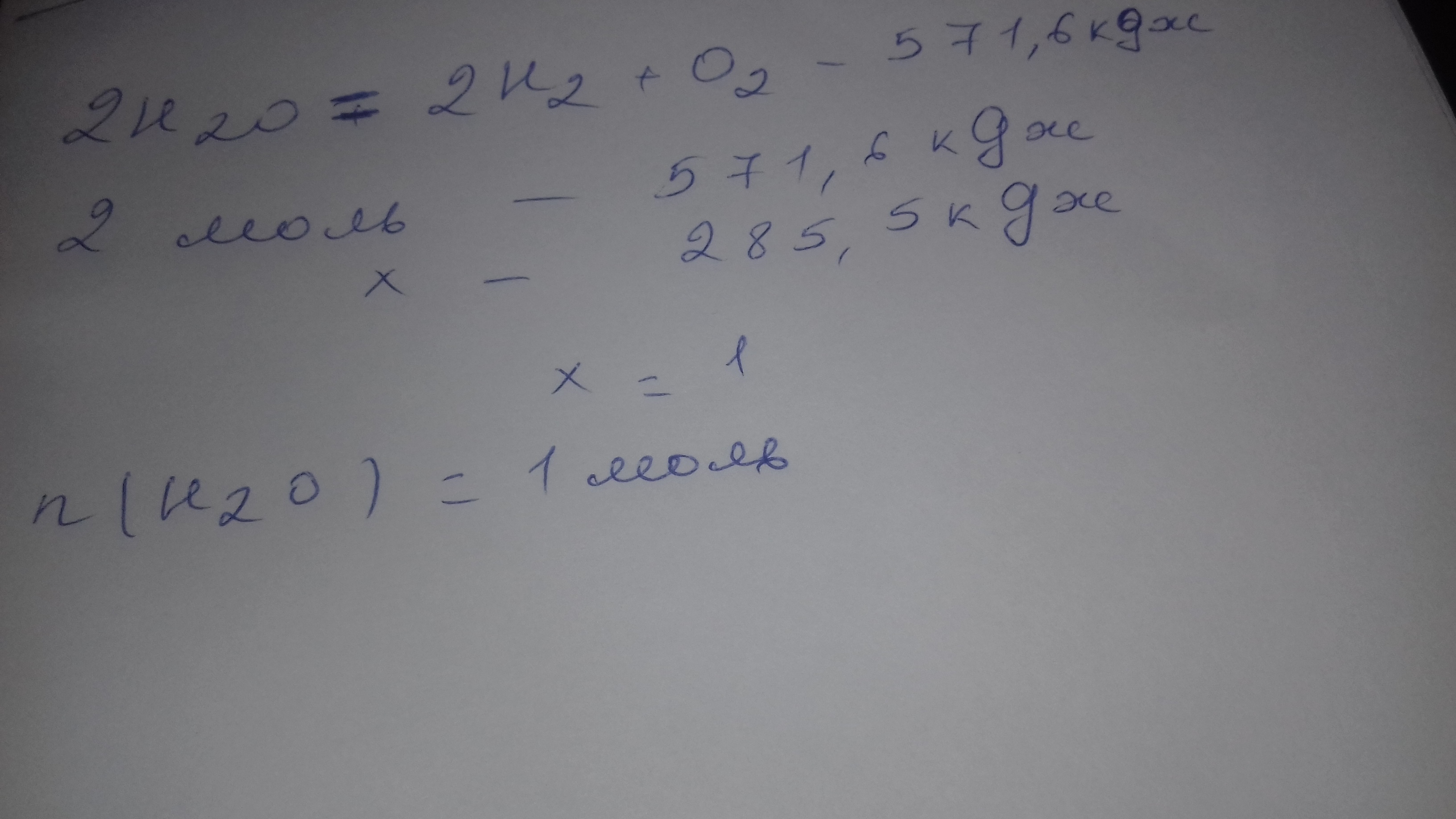
Ответил Senpoliya
0
Дано:
Qр-ции = -571,6 кДж
Q = -285,5 кДж
-----------------------------
η(Н₂O) - ?
Решение:
2Н₂O = 2H₂ + O₂ - 571,6 кДж
на разложение 2 моль Н₂O затрачивается 571,6 кДж
на разложение х моль Н₂O затрачивается 285,5 кДж
х = 2 моль * (-285,5 кДж) : (-571,6 кДж) = 1 моль Н₂O разложится
----------------------------------------------------------------------------------------------
Qр-ции = -571,6 кДж
Q = -285,5 кДж
-----------------------------
η(Н₂O) - ?
Решение:
2Н₂O = 2H₂ + O₂ - 571,6 кДж
на разложение 2 моль Н₂O затрачивается 571,6 кДж
на разложение х моль Н₂O затрачивается 285,5 кДж
х = 2 моль * (-285,5 кДж) : (-571,6 кДж) = 1 моль Н₂O разложится
----------------------------------------------------------------------------------------------
Приложения:
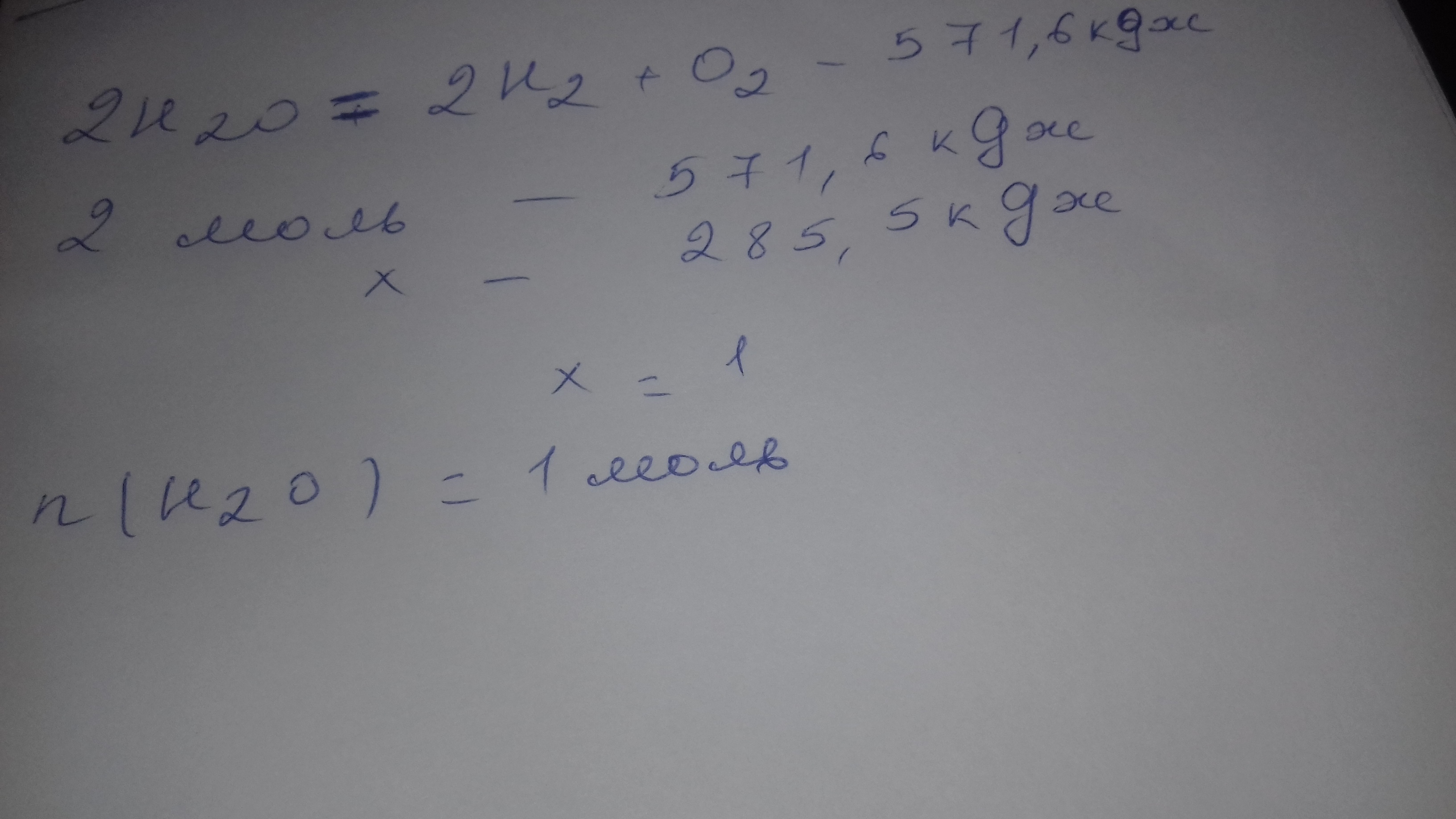
Ответил Аноним
0
подскажите
Новые вопросы
Геометрия,
2 года назад
Английский язык,
2 года назад
Алгебра,
8 лет назад
География,
8 лет назад
Математика,
9 лет назад